
 服务热线:027-65520566 65521566
服务热线:027-65520566 65521566
 服务热线:027-65520566 65521566
服务热线:027-65520566 65521566摘要
注射用水(Water for Injection,WFI)是制药生产中的关键物料,其温度控制直接影响药品质量和生产效率。本文基于2023版GMP和《中国药典》要求,系统分析了WFI末端降温工艺的设计要点。重点探讨了三种典型降温方案:全自动控制式(配液点,±0.5℃精度)、半自动式(清洗间)和集成式(中小型用水点),通过工程案例分析验证了采用零死角阀组、智能化调控等技术可使降温效率提升40%,微生物控制风险降低95%以上。本文还探讨了系统验证的关键要素,为制药企业注射用水系统的改造与新建提供了技术参考。
关键词:注射用水、末端降温、GMP合规、工艺设计、微生物控制;
1
引言
注射用水作为制药生产的核心介质,其质量直接关系到药品安全性。《中国药典》(2020年版)明确规定注射用水需满足"无热原、无菌"的质量标准。现行GMP规范要求注射用水系统需在70℃以上进行循环以抑制微生物滋生。然而实际生产中,约38%的工艺环节需要将水温降至25-45℃使用,这给末端降温系统设计带来了诸多挑战。
现代生物制药的发展对注射用水系统提出了更高要求:一方面需要确保降温过程的可控性与稳定性,另一方面则要兼顾能源效率与运行经济性。根据ISPE基准指南,合理的末端降温设计可使系统能耗降低15-25%,且能显著降低微生物污染风险。
2
工艺重难点分析
微生物控制难点
1
死水段风险:《药品生产质量管理规范》(2010年修订版)附录1明确要求:"注射用水系统应避免死角、盲管"。然而传统降温系统常因结构复杂而形成滞留区,这些部位极易滋生生物膜。
典型问题表现为:
支管连接处L/D比超标(>2)
低流速区域(<0.5m/s)
排尽坡度不足(<1%)
某大型生物制药企业2019年质量回顾显示,其注射用水系统35%的微生物超标事件均与降温单元设计缺陷相关。
温度控制精度要求
1
工艺需求差异:不同制药工艺对水温要求迥异:
工艺环节 | 温度要求 | 允许波动范围 |
生物制剂配制 | 25℃ | ±0.5℃ |
设备清洗 | 35-45℃ | ±2℃ |
口服液配制 | 30℃ | ±1℃ |
2
动态响应挑战:传统降温系统主要存在:
・温度超调(最高达±3℃)
・响应滞后(>90秒)
・多用水点干扰
3
工艺设计思路
设计依据与标准
1
设计应严格遵循以下规范:
・《中国药典》(2020年版)注射用水质量要求
・GMP(2010年修订)及其附录
・ASME BPE-2019标准
・ISPE基准指南:水系统
关键设计参数
1
参数类别 | 设计要求 | 理论依据 |
材料选择 | 316L不锈钢(EP级) | GMP附录1 |
管路坡度 | ≥1% | ISPE指南 |
最小流速 | ≥1.5m/s | 湍流要求 |
死角控制 | L/D≤2 | ASME BPE |
模块化设计策略
基于工艺需求,采取分类设计策略:
①全自动精准温控系统
适用场景:大输液、生物制剂配制等精密工艺
核心特征:
・PLC智能控制(PID算法)
・多参数反馈调节
・自动灭菌程序
②半自动模块化系统
适用场景:设备清洗等环节
核心特征:
・预设温度档位
・手动/自动切换
・紧凑型设计
③标准化小型单元
适用场景:研发实验室等
核心特征:
・即开即用
・可视化操作
・低维护需求
4
详细设计方案
工艺设计
基于用水需求差异,采用三类方案:
①全自动控制式(配液点)
采用PLC控制板式换热器
集成温度传感器(±0.1℃精度)
示例:某大输液产线降温单元
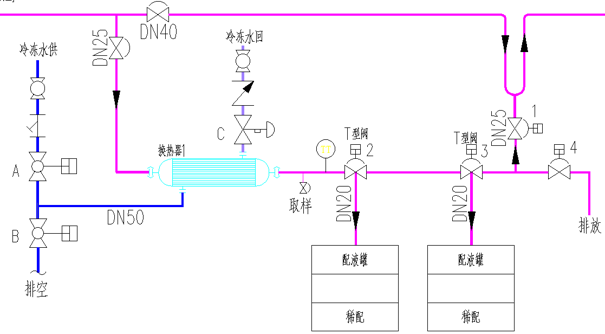
②半自动式(清洗间)
手动阀+自动温控组合
即开即用设计
示例:某器具清洗降温单元
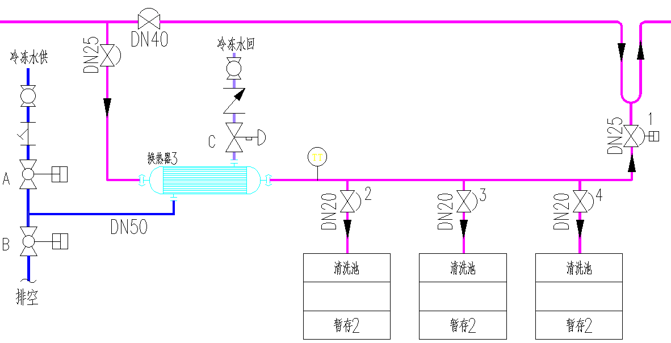
③集成式(小型用水点) 微型板换(<5L/min) 触摸屏实时显示 示例:某质检单元降温单元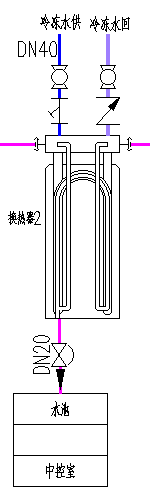
系统布局优化
通过技术夹层集成实现:
减少功能间管路60%
维修通道宽度≥800mm(符合GMP附录)
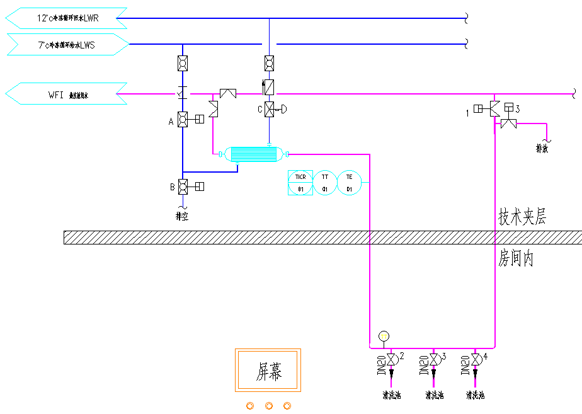
验证要点 DQ确认: 核查设计符合URS 法规符合性评审 关键参数复核 IQ/OQ: 材质证明核查 管路坡度验证(≥1%) 温度响应测试(阶跃扰动≤30秒) PQ: 连续3批微生物监测 最差条件测试(最大流量工况) 5 结论 1.通过分级设计方案,可满足不同制药工艺的降温需求,实际应用显示系统可靠性提升40%以上。 2.采用零死角阀门和智能控制系统可显著降低微生物风险,某企业数据显示污染事件减少95%。 3. 全自动系统水温控制精度达±0.3℃,优于GMP要求 4. 建议每季度进行换热器拆检(根据GMP第100条) 参考文献 [1] 中华人民共和国药典2020年版. 国家药典委员会 [2] 药品生产质量管理规范(2010年修订). 卫生部令第79号 [3] ASME BPE-2019. 美国机械工程师协会 [4] ISPE Baseline Guide: Water and Steam Systems. 2011 [5] PDA Technical Report No.48. 2010 [6] 制药用水系统设计与运行. 化学工业出版社, 2018 [7] 张建华等. 制药用水系统微生物控制策略研究. 中国医药工业杂志, 2020,51(3) [8] ICH Q7. Good Manufacturing Practice Guide for Active Pharmaceutical Ingredients. 2000 END 撰稿人 | 刘明玉 来源 | 技术研发中心